의약품 개발 과정
페이지 정보
작성일 24-06-03 15:23본문
우리가 병원에서 쉽게 처방 받고, 약국에서 손쉽게 접할 수 있는 의약품은 수많은 사람들의 노력과 시행착오를 통해 출시되게 됩니다. 이렇게 만들어진 의약품이 처음 출시되면 우리는 그 약을 ‘신약’ 이라고 합니다. 오늘은 그 신약의 개발 과정을 알아보도록 하겠습니다.
신약개발의 과정은 발견단계의 Discovery와 개발단계의 Development로 나뉩니다.
발견단계에서는 타겟 질병의 종류를 먼저 정하고, 세포 실험 및 동물 실험 등을 통해 신약후보물질을 도출하게 됩니다.
치료가능성이 있는 질병원인과 타겟을 규명하여 선택한 후, 기대하는 치료효과를 발휘할 수 있는 새로운 물질을 만들거나 기존에 만들거나 기존에 알려진 물질의 구조를 변경하여 신약후보물질을 선정하게 됩니다. 이 후보물질은 다양한 동물에 대해 실험적으로 안전성과 유효성을 시험하여 사람에게 임상시험을 실시하여도 안전하며 유효한지를 판단하게 됩니다.
이 후 개발단계에서 사람에서의 안전성과 유효성을 확인하는 임상시험을 실시하게 됩니다. 개발단계에서 실시되는 임상시험은 사람에게 사용되는 만큼 안전성과 윤리성이 보장되어야 하기 때문에 임상시험 전 식약처로부터 임상 시험계획에 대한 승인을 받아야합니다.
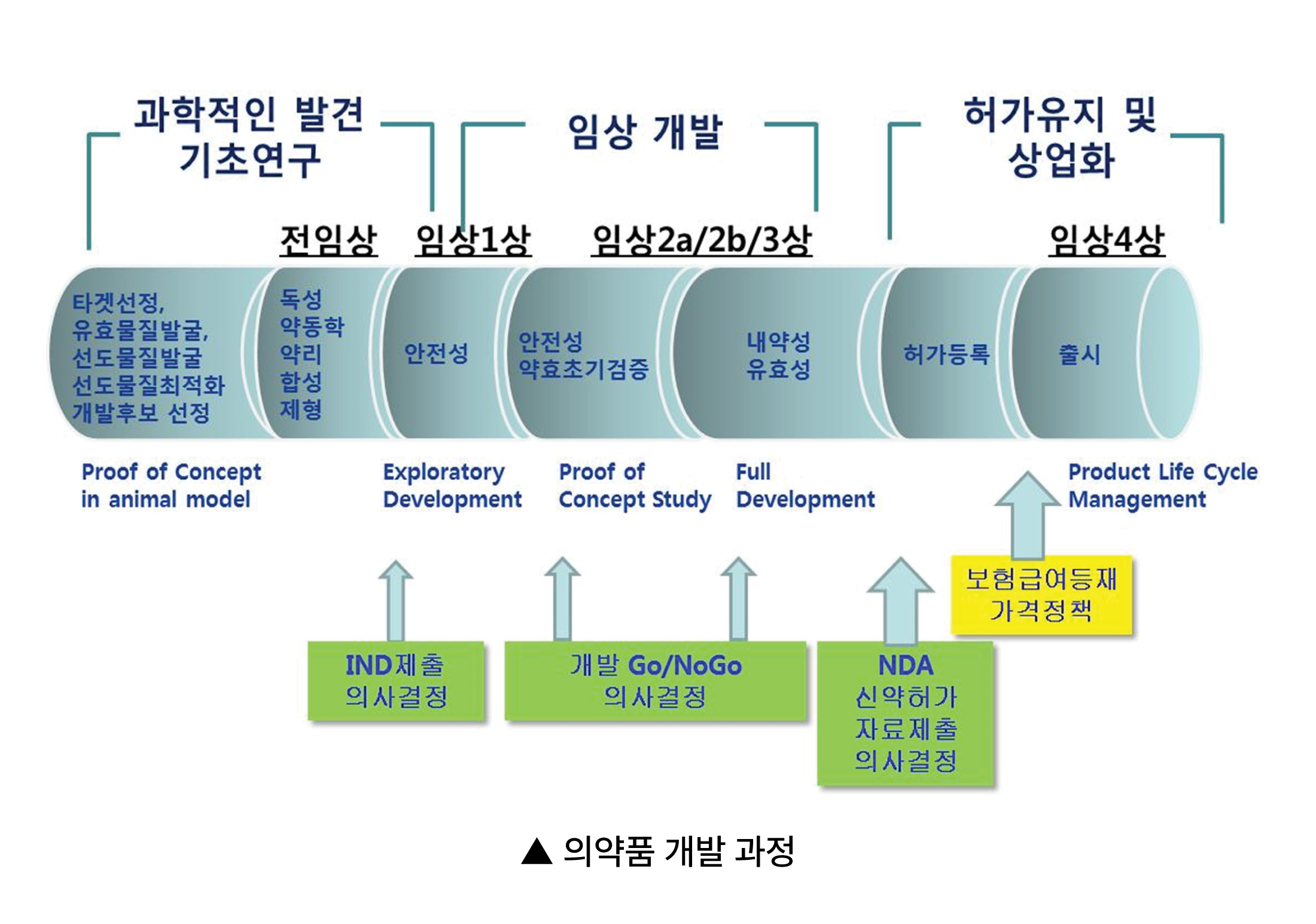
임상시험은 1상, 2상, 3상으로 나뉩니다.
먼저, 임상1상시험은 소규모(약 20명에서 100명)의 건강한 지원자를 대상으로 시험하는 단계로서, 의약품이 사람에게서 안전한지 여부를 확인하는 것을 목적으로 실시됩니다.
안전성이 확인되면 임상시험용 의약품이 기대된 작용기전(mechanism)에 따라 작용되는지 검토하고, 의약품을 사용에 있어서 최적 용량(dose strength)과 투약방법(schedules)을 확인하게 되는데 이를 2상이라고 합니다. 3상 시험은 대규모 환자를 대상으로 하며 후보 의약품의 안전성과 유효성 및 전체적인 benefit-risk 관계에 대한 통계학적으로 유의한 데이터를 만들기 위해서 약 1,000명에서 5,000명의 환자를 대상으로 연구를 실시하게 됩니다.
이 단계는 의약품으로서 안전성과 유효성 여부결정의 핵심단계로서 적정한 의약품 사용을 보증하기 위한 다른 의약품과 상호작용 정보 등 표시사항의 기초가 됩니다.
임상시험동안 실생산 규모의 생산계획, 식약청에 품목허가를 받기 위해 필요하고 복잡한 서류준비 등을 위한 품질등에 관한 중요한 연구가 많이 수행됩니다.
유효물질 수준에서 5,000개에서 10,000개의 화합물이 연구개발(R&D)의 파이프라인으로 들어가지만 전임상단계에서 약 250개의 연구를 거쳐 결국 1개의 승인을 받게 됩니다. 이러한 신약개발 과정을 거쳐 환자가 이용할 수 있을 때까지 소요되는 기간과 비용은 약 10년~15년의 연구개발기간과 비용은 800백만달러에서 13억달러($1.3 billion)이상으로 추정될 정도로 많은 비용과 기간이 소요됩니다.
참고: https://nedrug.mfds.go.kr/cntnts/4


